Uten noen forseelse mot de andre anatomiske strukturer som er involvert, kan vi si at hele kardiovaskulærsystemet eksisterer med det eneste formål å betjene kapillærene. Det er på dette nivået faktisk at ovennevnte utveksling av næringsstoffer, hormoner, antistoffer, gasser og alt som overføres av den hematiske strømmen, finner sted. Cellene derimot, er avhengige av kapillærernes evne til å forsyne alle elementene som er nødvendige for deres metabolisme, samtidig som de fjerner avfallet som vil forgifte dem. Men hva styrer dette avsnittet?
Utveksling av stoffer fra kapillærene til celler kan i hovedsak være av tre typer.
A) Den første er representert ved diffusjonen . Typisk av gasser, reflekterer den netto bevegelse av molekyler fra punktet med størst konsentrasjon til det ved en lavere konsentrasjon; denne strømmen fortsetter til molekylene er jevnt fordelt i hver del av ledig plass. Flertallet av utvekslingen mellom plasma og interstitial væske oppstår ved enkel diffusjon, som involverer stoffer som ioner, lavmolekylære molekyler, aminosyrer, glukose, metabolitter, gasser, etc.; men de filtrerer ikke molekyler med en molekylvekt på mer enn 60kD, slik som store proteiner og blodkropper (hvite, røde blodlegemer, etc.). Spesielt passerer de fettløselige stoffene gjennom plasmamembranene, og utvekslingen er begrenset av hastigheten på blodstrømmen; De vannløselige, derimot, passerer gjennom små porer, og deres strømning reguleres av bredden av disse porene og av radiusen til molekylet som vurderes.
Diffusjonsmekanismen blir mindre effektiv i nærvær av ødem, fordi den høye mengden interstitial fluid øker avstanden mellom vev og kapillær.
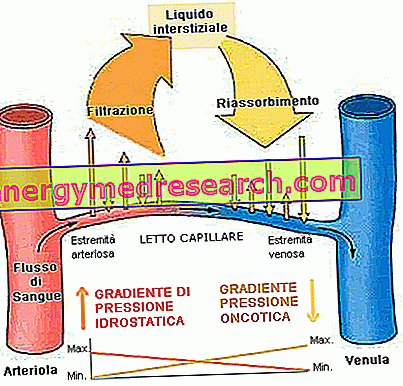
B) En annen type utveksling er gitt av filtreringsreabsorbsjonssystemet, som - også kjent som massestrøm - regulerer hovedsakelig passasjen av væsker. Hvis strømningsretningen er orientert mot utsiden av kapillærene, snakker vi om filtrering, mens når den er rettet mot interiøret, snakker vi om absorpsjon.
Reguleringen av denne strømmen avhenger av tre faktorer: det hydrauliske eller hydrostatiske trykket, det onkotiske eller kolloid-osmotiske trykket og permeabiliteten til kapillærveggen.
- For noen få linjer siden minnet vi om at det hydrostatiske trykket ved kapillærens arterielle ende er rundt 35 mm Hg, mens det ved den venøse enden er omtrent halvparten. Disse verdiene reflekterer det laterale trykket som utøves av blodstrømmen, som har en tendens til å presse væsken ut gjennom selve kapillærens vegger. Tvert imot favoriserer det hydrostatiske trykket som utøves av den interstitielle væsken (estimert ved 2 mm Hg) den motsatte bane, presser mot kapillærveggen og favoriserer innføringen av væsker inne i den.
- Den andre faktoren, det onkotiske trykket, er strengt avhengig av konsentrasjonen av proteiner i de to rom. Disse har faktisk en meget lignende sammensetning, bortsett fra plasmaproteiner, som er nesten fraværende i interstitialvæsken. Det onkotiske trykket representerer kraften som regulerer passasjen av vann ved enkel diffusjon fra "proteisk" mindre konsentrert til det mer konsentrerte rommet, gjennom en semipermeabel membran mellom dem (som tillater vann å passere gjennom det, men ikke fra proteiner som er tilstede i den) og gitt i dette tilfellet av kapillærveggene.
Det onkotiske trykket som utøves av proteinene som er tilstede i blodet, er lik 26 mm Hg, mens det i interstitialvæsken er nesten ubetydelig.
- Den tredje og siste faktoren er representert ved den hydrauliske konduktansen, som uttrykker vannpermeabiliteten til kapillærveggen. Denne størrelsen varierer i henhold til de morfologiske egenskapene til kapillærene (for eksempel er den større i de fenestrerte, typiske for nyrene).
Disse tre elementene er artikulert i Starlings lov:
kapillærutveksling er avhengig av en konstant hydraulisk konduktans multiplikert med forskjellen mellom den hydrostatiske trykkgradienten og den kolloidosmotiske trykkgradienten.
STARLINGSRETT Jv = Kf [(Pc - Pi) - σ (ppc-ppi)]
Ved den arterielle enden av kapillæren ville vi ha et nettofiltreringstrykk på:
| [(35 - (- 2)] - (25-0) = 12 mm Hg | dette presset forårsaker utslipp av væsker og metabolitter tilstede i blodet (filtrering oppstår) |
Langs passasjen i kapillærene blir hastigheten og hydraulisk trykk redusert på grunn av friksjon. Onkotisk trykk har en tendens til å forbli det samme, unntatt når kapillærveggene er ganske permeable for proteiner med lav molekylvekt. Denne egenskapen har viktige konsekvenser, siden den reduserer det kapillære onkotiske trykket, øker interstitialen. For å ta denne muligheten i betraktning, ble Laplace's lov korrigert ved å sette inn den såkalte refleksjonskoeffisienten (σ), slik at: Jv = Kf [(Pc - Pi) - σ (ppc-ppi)].
Refleksjonskoeffisienten varierer fra 0 (kapillærvegg helt permeabel for proteiner) til 1 (kapillærveggen ugjennomtrengelig for proteiner).
Ved den venøse enden av kapillæren ville vi ha et nettofiltreringstrykk på:
| [(15 - (- 2)] - (25-0) = -8 mm Hg | dette trykket fører til at væsker og cellulære metabolitter kommer inn i blodet (reabsorpsjon oppstår). |
MERK: det lavere reabsorpsjonstrykket kompenseres av kapillærens større permeabilitet til venøst hode; Til tross for dette er det filtrerte volumet fortsatt større enn det som reabsorberes. Faktisk reabsorberes kun 90% av det filtrerte volumet ved arterieenden til det venøse De resterende 10% (ca. 2 l / d) gjenvinnes av lymfesystemet, som forhindrer dannelsen av ødem ved å helles i blodet.
Trykkverdiene som er vist i eksemplene er veiledende og er ikke sjeldne unntak. Kapillærene som utgjør glomeruli av nyrene, for eksempel, har en tendens til å filtrere langs hele lengden, mens noen kapillærer som er tilstede på nivået av tarmslimhinnen, bare absorberer, samler næringsstoffer og væsker.
C) Den tredje mekanismen kalles transcytose og er ansvarlig for transporten av enkelte molekyler med høy molekylvekt, slik som visse proteiner som etter at de er innlemmet i vesikler ved endocytose, passerer gjennom epitelet og frigjøres i interstitialvæsken ved eksocytose.



