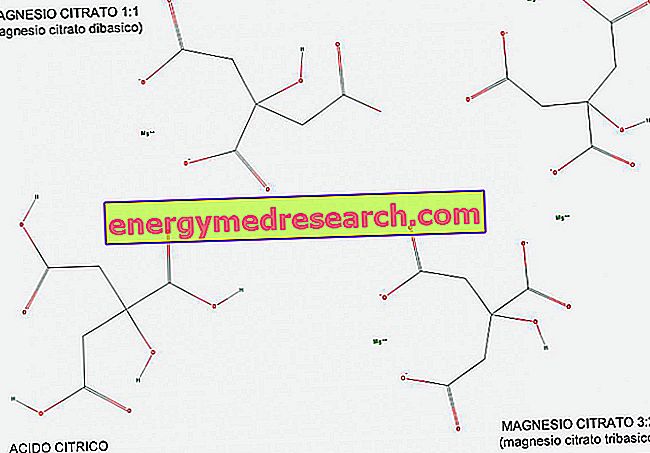
En tribasisk (eller triprotisk) syre er en syre som har tre hydrogenioner å donere i en syrebasereaksjon. Med hjelp av figuren kan vi se hvordan sitronsyre er et eksempel på tribasinsyre, da den har tre COOH karboksylgrupper som enkelt kan overføre hydrogen H.
Magnesiumsitrat finnes i både en 1: 1-andel (1 magnesiummolekyl pr. Sitratmolekyl) og i en 3: 2-andel (3 magnesiummolekyler pr. 2 molekyler citrat).
1: 1 magnesiumcitrat kalles dibasisk fordi det er et dibasisk salt av sitronsyre; Faktisk har den 2 univalente basiske grupper (COO-) per molekyl, avledet fra de 2 karboksylgrupper som har gitt opp hydrogen under reaksjonen.
3: 2 magnesium, derimot, kalles tribasisk fordi den har 3 univalente basiske grupper (COO-) per molekyl, avledet fra de 3 karboksylgrupper som ga opp hydrogenet under reaksjonen.
Tribasisk magnesiumsitrat er tydeligvis rikere i magnesium (+ 42, 6 vekt%) enn dibasisk magnesiumcitrat; Dessuten er det mer alkalisk, siden det kan akseptere tre hydrogenioner H + mot de to som er akseptert av dibasisk. Men det er mindre løselig i vann.



